
27岁男性,膀胱囊实性占位病变,泌尿系肿瘤?答案并非如此。
【病例资料】
患者男性,27岁,因“体检发现左肾积水10月”入院。
入院查体
腹软,无压痛反跳痛,未触诊包块及肿物,左侧肾区轻度叩痛,左侧输尿管下段行经区明显压痛。
实验室检查
血、尿常规及肝功能检查未见明显异常;肾功能:肌酐126.0 μmol/L,尿素氮5.82 mol/L。
辅助检查
B超提示:左肾积水,左输尿管扩张,膀胱左下方4 cm×4 cm的囊实性占位病变。
CT示:左肾盂肾盏及输尿管近全程扩张;左输尿管膀胱入口区可见一4 cm×4 cm×5 cm的囊状低密度影,左侧精囊腺增大,与占位关系密切(图1);膀胱形态正常,壁光整,未见明显增厚。
肾动态结果:右侧40.1 ml/min,左侧7.3 ml/min。
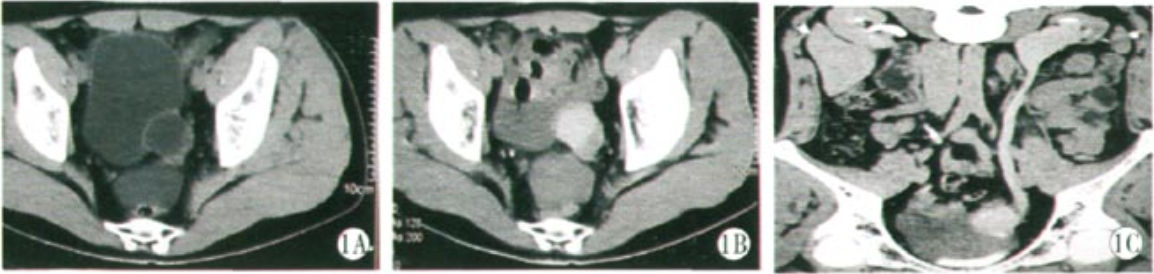
图1:盆腔侵袭性纤维瘤CT图像
A:增强期;B:延迟期;C:延迟期三维重建。
【诊疗经过】
人院后行输尿管镜检查+剖腹探查术:输尿管镜进入左侧输尿管约3 cm见管腔明显变窄,似有肿物外压;改行剖腹探查,取左下腹斜切口,术中于髂血管分叉远端3 cm处见软组织肿物,大小约3 cm×4 cm×2 cm,质硬,灰白色,压迫膀胱,包绕输尿管,并与左侧精囊粘连,沿肿块周围一并切除肿块、输尿管下段、部分折返腹膜及左侧精囊,行输尿管膀胱再吻合。
病理检查结果:盆腔肿物4 cm×3 cm×2.5 cm。
镜下可见:精囊腺、输精管浆膜外及被覆移行上皮的平滑肌组织中可见增生的纤维组织呈浸润性生长(图2)。

图2:袭性纤维瘤组织病理(HE×10)
左输尿管末端镜下:被覆移行上皮的平滑肌组织外可见增生的纤维组织呈浸润性生长。
免疫组化:Vim(+)、S-100(一)。
诊断:(盆腔)侵袭性纤维瘤病。
术后予以局部放疗,随访3月未见复发。
【讨论】
关于侵袭性纤维瘤(AF)
1.流行病学特征
硬纤维瘤病由MULLER于1838年首次提出并命名,是一种生长缓慢、无远处转移、局部侵袭性及复发率较高的交界性肿瘤。该病多见于腹壁及四肢,而发生于盆腔或泌尿系统周围的少见,由于容易累及输尿管、膀胱及卵巢,多被误诊为泌尿系或妇科肿瘤。
AF好发于30~40岁,男女比例在1:2~5。常是无意中发现躯干、四肢不能推动且无波动的硬性肿块,或因压迫相邻器官引起相关症状而就诊。杨晓坤等报告4例表现为泌尿系疾病的AF,其中2例侵犯输尿管引起肾积水,另外2例分别侵犯肾脏和膀胱。
2.病因
该病病因尚不清楚,可能与遗传、内分泌、外伤以及基因等因素有关。AF患者中大约有10%~15%同时患有家族性腺瘤样息肉病,认为家族性腺瘤样息肉病的基因突变能诱发AF的发生。SKUBITZ等通过基因分析发现,ADAMl2、WISP-1、SOX-11和成纤维细胞活化因子-a在侵袭性纤维瘤组织中明显高表达,认为在发病过程中发挥重要作用。此外文献报道,雌激素及创伤均可能是本病的促发因素
3.诊断
AF源于肌肉、腱膜、深筋膜等纤维组织。肉眼观形态不规则,无包膜,呈浸润生长。病变质硬,切面灰白,并可见编织状排列的纤维束。显微镜下见大量胶原纤维中衬有极少的纤维母细胞和肌纤维母细胞,它们排列成束,界限不清,细胞可见异形性和核分裂相。超微结构可见应力纤维,纤维连接复合体,中间连接以及缝隙链接;细胞部分被基质包绕。免疫组化显示高表达波形蛋白(Vim),而酸性二聚体钙结合蛋白(S-100)、CD34极少表达。
影像学检查有助于肿瘤的定位及浸润范围的判断,但对于该病的诊断缺乏特异性。AF在CT平扫影像上的密度比肌肉密度略低,使用造影剂后病灶强化,但对鉴别AF与其他软组织的肿瘤作用不大。B超表现为低回声团块,可呈分叶状,无包膜,边界欠清晰,与周围组织关系紧密。彩色多普勒血流显像:肿瘤血流较丰富,尤其边缘明显。MRI图像表现具有一定特征性,T1WI呈较均匀的低信号或中高信号;T2WI呈现不均匀的高信号,高于肌肉而低于皮下脂肪,并可见点状、条状低信号带;增强显像明显,提示肿瘤血供丰富。最近RAMOS等报道,18F一氟脱氧葡萄糖一PET/CT技术可发现微小的浸润和残存病灶,指导手术切除和放疗范围。
4.治疗
由于AF具有局部侵犯、高复发的生物学特点,目前选择以手术为主的个体化综合治疗。
手术切除是最为有效的治疗方法。行肿瘤广泛切除,即完整切除肿瘤及肿瘤周围2~3 cm的正常组织。目前多数学者认为,手术切缘与肿瘤复发明确相关,切缘阳性较切缘阴性患者术后复发几率明显增高。对于局部复发的肿瘤,可再次手术切除,但术后再复发率明显增高。对于切缘阳性的患者,术后辅助放疗具有较好的效果。有学者认为,放疗并不能降低术后局部复发率,且带来很多并发症,甚至有诱发局部恶性肿瘤的可能。建议对首次切缘阴性的患者术后可加强随访,暂不放疗。但对于两次复发的患者,再次手术切缘即使为阴性,仍具有高达50%的局部复发率,所以针对这部分患者,仍主张术后尽早辅助放疗。
由于手术和放疗对AF具有良好的治疗效果,目前化疗仅限于不宜手术和放疗的病例。
CAGLAR等幻报道应用小剂量的长春碱和甲氨蝶呤联合治疗手术无法完整切除的侵袭性纤维瘤,随访75个月,有60%的病例肿瘤无进展或体积明品减小。另有报道部分AF表达雌激素受体,应用抗雌激素如他莫昔芬等药物治疗有效。最近,RAVAIOL等报道酪氨酸激酶拮抗剂甲磺酸伊马替尼对腹壁型侵袭性纤维瘤具有一定疗效。
5.预后
尽管本病有局部侵袭性强、术后易复发的生物学行为,但存活率较高,5年存活率在90%以上。对于复发率,文献报道不一,多在24%~72%之间。可能影响复发的因素包括:患者年龄和性别,肿瘤部位、大小,肿瘤性质(初发或复发),手术切缘,辅助放疗范围和剂量等。
盆腔AF临床罕见,生物学行为发展缓慢,局部浸润性强,易复发,侵犯泌尿系统时易被误诊为泌尿系肿瘤。结合临床表现及影像学特点应考虑到盆腔AF的可能,最终诊断依据病理。治疗采取以手术为主的个体化综合治疗。
来源:李炫昊,刘庆军,杜林栋.盆腔侵袭性纤维瘤致输尿管狭窄1例报告并文献复习(J).现代泌尿外科杂志,2010,15(3):210-211.