
01病例资料
患者男性,17岁,于2022年2月1日 因“右侧睾丸疼痛伴坠痛2d”为主诉入院。入院时患者右侧睾丸红肿,明显肿大,约8cm×5cm×5cm,质硬,睾丸、附睾界限不清,透光实验阴性,抬举试验阳性,睾丸附睾触痛阳性;左侧睾丸未见明显异常。超声检查显示:右侧阴囊壁增厚,约13mm;右侧睾丸回声欠均,外上方结构紊乱,可见形态不规则的低回声区,范围约68mm×46mm×31mm,内回声明显不均,似可见体积增大的附睾及精索回声,于右侧睾丸周围可见深约8mm的液性暗区。彩色多普勒血流及能量图显示:右侧睾丸未见明显血流信号,外上方低回声区内血流信号丰富。超声检查报告:右侧睾丸外上方低回声区,性质待定,考虑“恶性肿瘤?”;右侧睾丸扭转、阴囊壁水肿,周围少量鞘膜积液(图1A)。尿液分析+尿沉渣检查示:潜血(+++),蛋白质(+),红细胞246.40个/μl。血液分析:白细胞计数(WBC)15.61×109/L,中性粒细胞比例78.20%,淋巴细胞比例15.20%,嗜酸细胞比例0.10%,中性粒细胞计数12.21×109/L,单核细胞计数0.99×109/L,嗜酸细胞计数0.01×109/L;心肌酶、人绒毛膜促性腺激素、甲胎蛋白、凝血功能、术前八项等均无明显异常。
根据患者病情判断,目前症状只能经手术治疗缓解,且未见明显手术禁忌证,遂于入院当日行急诊手术,术式暂定为右侧睾丸探查+右侧睾丸切除+左侧睾丸固定术。患者全麻成功后,从右侧睾丸逐步切开皮肤、肉膜,见各层组织间炎症、水肿明显,粘连严重;游离睾丸鞘膜囊,纵行切开囊壁,见囊壁明显增厚,充血水肿;睾丸、附睾与周围组织粘连严重;探查见右侧精索逆时针旋转180度,睾丸、附睾及精索明显水肿、淤血、颜色发黑;将精索、睾丸、附睾复位,温盐水及利多卡因注射液湿敷30min,睾丸、附睾颜色无好转,术中超声检查提示右侧睾丸、附睾无血流(图1B),遂行右侧睾丸切除术,将睾丸、附睾及部分精索完整切除(图1C)。考虑到右侧阴囊内炎症反应明显,为避免左侧睾丸感染,暂不行左侧睾丸固定术。术后病理报告(部分):(1)肉眼观睾丸周围见一肿物,大小约9cm×7cm×5cm,切面实性灰白、灰黄色,质硬,界不清;(2)病理诊断胚胎性横纹肌肉瘤,局部细胞间变,肿瘤浸润睾丸周围软组织、附睾及精索组织,局部浸润睾丸,可见脉管内瘤栓(CD34)及神经周围浸润(图1D、E、F)。患者于2022年2月7日出院后未再复诊,失访。
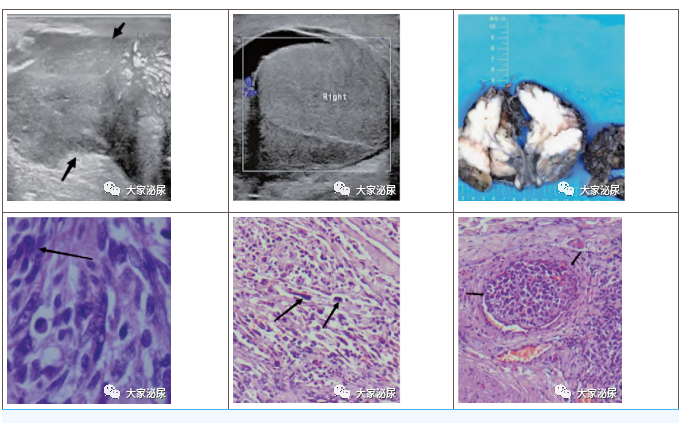
A:B超检查示:睾丸周围可见一低回声区,边界不清,形态不规则(箭头所示);
B:术中B超检查示:右侧睾丸生理位置发生改变,其内未见明显血流信号,提示扭转伴坏死;
C:术中切除物:可见右侧睾丸切面灰褐、灰红色,质地中等;睾丸周围肿物切面实性,灰白、灰黄色,质硬;
D:病理切片中可见肿瘤细胞(箭头所示)(HE染色,×400);
E:病理切片见局部肿瘤细胞间变,肿瘤细胞缺乏分化、异型性显著(箭头所示)(HE染色,×200);
F:病理切片见脉管内瘤栓,肿瘤周围血管内可见癌细胞浸润(箭头所示)(HE染色,×200)。
图1 病例的超声检查、术中切除物及病理结果
02讨论
横纹肌肉瘤是儿童期最常见的软组织肿瘤,它是由不同分化程度的间叶源性细胞组成,且恶性程度较高,其组织类型可分为胚胎性、腺泡状、多形性或间变性3个亚型。胚胎性横纹肌肉瘤可发生于头颈部、四肢等全身各个部位,其中眼眶是最常见的部位,但是生长在睾丸、附睾及精索的临床病例较为罕见,并且位于睾丸旁的发生率仅占所有阴囊内横纹肌肉瘤的7%。睾丸旁横纹肌肉瘤可通过淋巴途经转移至腹膜后淋巴结及腹主动脉旁淋巴结,也可以通过血管途经进行转移,其中肝和骨是最常见的转移部位。
睾丸旁横纹肌肉瘤通常表现为阴囊内或腹股沟管内出现短时间增大的单侧无痛性肿块,或非特异性症状,如食欲下降、疲劳、体重减轻,出现睾丸疼痛和鞘膜积液的患者在临床上极为罕见,仅见个例报道。本文报道的患者临床表现为单侧睾丸疼痛伴坠痛,且发病前并未发现阴囊内有无痛性肿块;其临床症状出现是由于肿物压迫了神经,且本身伴有睾丸扭转并部分坏死,可能还存在阴囊内炎症导致鞘膜积液的出现,因此,给疾病的诊断带来了一定干扰,极容易与单纯睾丸扭转、单纯附睾炎相混淆。
目前,超声检查是该疾病诊断的首选手段。但是睾丸旁横纹肌肉瘤的彩色多普勒超声表现容易与附睾炎、腺瘤样瘤和平滑肌瘤相混淆。本病例中超声二维声像图显示右侧睾丸生理位置发生改变,彩色多普勒血流及能量图显示血流信号消失,提示扭转伴坏死;右侧睾丸外上方可见形态不规则的低回声区,内回声不均,体积较大,其内可见扭转的精索组织,但血流信号丰富,与单纯睾丸扭转表现不符,倾向于考虑富血供恶性肿瘤(图1A、B)。有研究发现,男性生殖系统的横纹肌肉瘤表现为血流信号较丰富的实性高回声团块,但也有表现为低回声的报道。我们认为团块超声回声特征不足以作为横纹肌肉瘤的特异性表现。临床考虑为睾丸旁横纹肌肉瘤等恶性肿瘤时,仅依靠临床症状及超声表现,极易误诊,尤其当患者同时伴有炎症存在或睾丸扭转时,因此,病理学检查仍是诊断的“金标准”。
局限性睾丸旁横纹肌肉瘤一般预后较好,但年龄≥10岁、肿瘤直径>5cm、累及淋巴结往往预示着预后不良。目前,该疾病的治疗方式仍存在较大争议,手术仍是主要治疗方法,术后根据个体化病情予以放射治疗、化学治疗等辅助治疗。睾丸肿瘤可能直接影响生殖功能、损害精子质量,手术等治疗方式也会在一定程度上损害生育力,放射治疗和化学治疗对生殖细胞的损伤更为显著。因为睾丸组织对辐射极其敏感,对侧的正常睾丸也会面临辐射损伤的风险,造成潜在的生育能力受损。随着医疗技术的发展以及患者对治愈后长期生存质量要求的提高,如何进行生育力保护逐渐成为个性化治疗方案的一部分。在治疗前和治疗过程中,临床医师应告知患者或未成年患者的父母治疗可能带来的生育力损害,与患者进行充分地沟通,在制定治疗方案时应考虑到生育力保护。目前,应用于临床的生育力保护手段主要有冷冻保存技术,如睾丸组织冷冻保存和精子冷冻保存等。
综上,本病例的诊疗过程提示,当患者存在睾丸疼痛且超声检查显示睾丸扭转伴睾丸旁血流丰富的团块时,不能忽略恶性肿瘤的存在可能;在临床实践中应进一步完善相关辅助检查,以尽早诊断和治疗,改善患者预后情况。
来源:张英檀、孙丽、李丽.《睾丸旁胚胎性横纹肌肉瘤伴睾丸扭转1例》[J].生殖医学杂志,2022,31(11):1598-1600.