
原发于肾脏的神经内分泌癌(NEC)十分罕见,是分化较差的上皮肿瘤,伴有神经内分泌分化,多发于肺脏、胰腺和胃肠道,在肾脏恶性上皮肿瘤中所占比例不足1%。本篇报道1例。
【病例资料】
患者女性,53岁,因体检发现右肾占位1月余入院。查体未见明显异常。
【实验室检查】
血常规、肝肾功能、乳酸脱氢酶、血钙正常。
尿常规:尿潜血(+)。
血沉:46 mm/h。
【辅助检查】
彩超
示右肾占位,大小约12.5 cm×15.7 cm,低回声块,内部回声尚均匀,肿块向外膨出,压迫肾窦,造影剂谐波成像呈“高增强、快消退”。
CTA+CTU
示右肾区巨大占位,最大截面约13.8 cm×12.7 cm,与肾上腺分界欠清,考虑为恶性病变可能大(图1)。
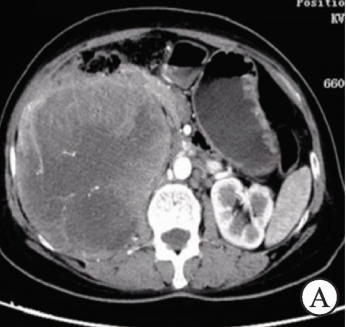
图1
PET/CT
示右肾区巨大软组织密度占位,代谢不均匀增高,考虑肾癌可能性大。
【诊疗经过】
初步诊断为右肾肿瘤。因瘤体较大,手术困难,先行选择性右肾动脉栓塞术。局麻下穿刺右侧股动脉,置入COBRA导管,将导管置入右肾动脉内。造影示右肾动脉分支稍增多、纤细、紊乱,可见包绕征象,实质期见巨大肿瘤染色。经导管于右肾动脉内注入栓塞微粒、明胶海绵颗粒适量及栓塞钢圈行栓塞治疗,复查造影上述征象消失。
2个月后,复查泌尿系CTA+CTU示右肾窝和腹膜后巨大囊实性占位,最大横截面积约14.3 cm×10.4 cm,考虑恶性病灶(图2)。
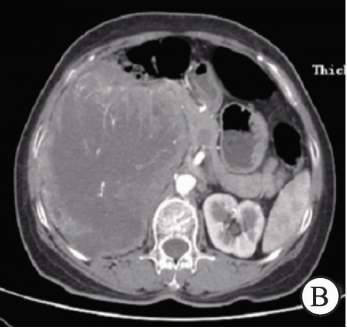
图2
全麻下行经腹右肾根治性切除术,术中所见:右肾见一椭圆形肿块,大小约17 cm×15 cm、境界不清、质地韧,与肝脏、膈肌、肾门、肾上腺界限不清,充分游离肾脏背侧,找寻并仔细游离肾动、静脉,分别用结扎并离断肾动、静脉。游离并结扎输尿管,因肿瘤与膈肌粘连严重,在保证肿瘤完整切除的前提下,部分膈肌破裂,予以修补,完整切除右肾、肿瘤和右侧肾上腺。
术后病理:右肾切除标本示结节样肿块1枚,大小17 cm×15 cm×15 cm,切面多彩状,实性、质软,表面大部分区被覆包膜、尚光滑,肿瘤组织累及肾盂,并穿透包膜累及周围纤维脂肪组织。神经见肿瘤组织侵犯;脉管内未见明确肿瘤栓子。显微镜下:组织内见片状、乳头状排列的异型细胞浸润性生长(图3)。
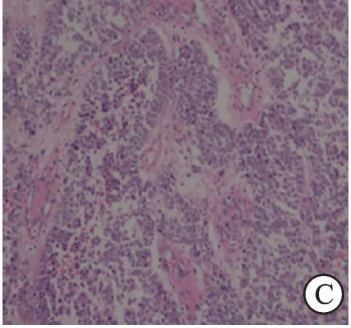
图3:肾实质肿瘤病理镜下图像(HE,×200)
免疫组化:CK(±),Vim(+),CK7(-),CD57(+ +),WT1(-),P63(-),34βE12(-),CD10(-),CD56(+ + +),Syn(-),CgA(+),TTF1(-),NSE(+),Ki67最密集处约10%(+)(图4)。病理诊断:右肾恶性肿瘤,结合免疫组化考虑神经内分泌癌。术后患者拒绝化疗,随访8个月未见复发,后失访。
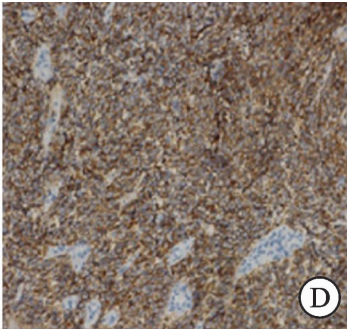
图4:肿瘤组织免疫组化-CD56阳性表达(Envision二步法,DAB显色,×200)
【讨论】
关于NEC
1.流行病学特点
NEC是分化较差的上皮肿瘤,伴有神经内分泌分化,多发于肺脏、胰腺和胃肠道,原发于肾脏者十分罕见,在肾脏恶性上皮肿瘤中所占比例不足1%。肾脏NEC多无特异性临床表现,好发于中老年人群,无明显性别倾向。
2.诊断
NEC在影像学上缺乏特异性,确诊主要依据病理学检查及免疫组化结果。最新WHO肾脏肿瘤分类(2016)将类癌归为高分化神经内分泌肿瘤,而小细胞癌和大细胞神经内分泌癌归为高级别NEC。镜下形态如下:
(1)高分化神经内分泌肿瘤:排列紧密,呈管状、条带状或巢状,肿瘤细胞规则一致,核仁不明显,核分裂罕见,坏死亦不常见。
(2)小细胞癌细胞:呈小圆或梭形,核仁缺乏或不明显,坏死常见。
(3)大细胞神经内分泌癌细胞:多为片状或巢状分布,细胞核较大,细胞质丰富,核仁明显,高级别NEC核分裂相多见。
常用的免疫组织化学标志物有嗜铬粒素A(CgA)、神经元特异烯醇化酶(NSE)、腺癌突触素(Syn)和CD56。CD56在肾NEC中常常表现为高表达,故当CD56为阴性时可作为一种排除性诊断的标记物。
3.治疗
目前,治疗肾脏NEC的首选方式是手术。以铂类为基础的化疗方案已用于肾脏NEC,但远期疗效尚不清楚。也有报道称,单纯接受化疗的NEC患者预后可能优于单纯接受手术或手术和化疗联合治疗的患者。本例在行根治性切除术前瘤体较大行肾动脉栓塞术以减少肿瘤血供,使肿瘤缺血坏死,引起周围组织肿胀,便于手术剥离。本例患者栓塞术后复查肿瘤未见明显缩小,但术中出血较少,降低了手术风险。
来源:刘贺,曹月鹏,郭宏骞,燕翔.肾脏神经内分泌癌1例报告(J).现代泌尿外科杂志,2017,22(9):727-728.