
泌尿系结石是泌尿外科的常见病,中国成年人尿石症的患病率为6.5%,而且复发率高,5年复发率可达50%,严重地威胁着患者的健康。近年来,治疗尿石症的微创技术发展较快,特别是软性输尿管镜术在我国得到广泛应用。但由于其操作复杂、手法精细、学习曲线相对较长,加之软镜价格昂贵,操作不当极易损坏镜体。因此,在临床上较易出现各种并发症。本篇着重介绍软性输尿管镜术的临床应用和并发症预防。
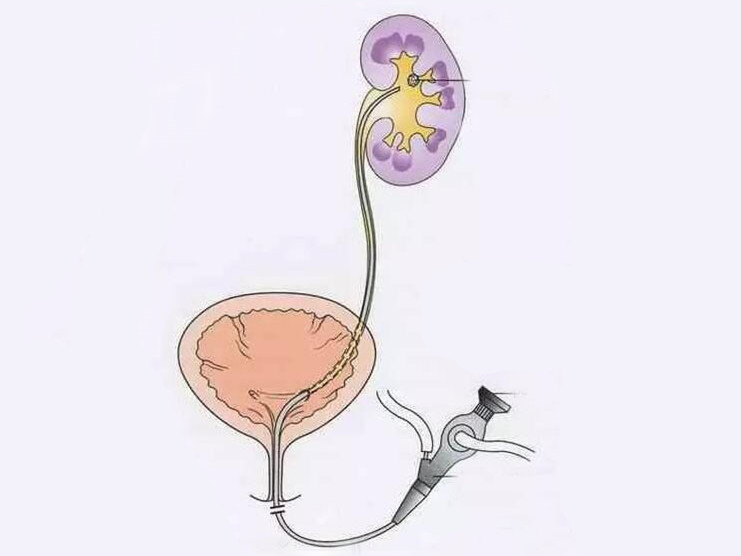
一、软性输尿管镜术的临床应用
1.软镜钬激光碎石术
软镜下钬激光碎石术用于治疗≤2 cm的肾结石,也可用于输尿管上段结石的治疗,对经皮肾镜取石术(PCN)术后残余结石可采用软镜钬激光碎石术,软镜可联合经皮肾镜治疗复杂性肾结石。对于肾结石直径>2 cm的病例,软镜钬激光碎石术可作为一种替代治疗,推荐分期手术。对于双肾<1.5 cm结石,同期双侧行软镜手术是安全的,且并发症少。
2.上尿路来源血尿的镜检和治疗
软性输尿管镜检术诊断性应用的适应证包括:①不明原因的上尿路来源血尿;②影像学上的充盈缺损;③尿道膀胱镜检查发现单侧或双侧上尿路血尿同时尿细胞学检查异常;④不明原因的输尿管或漏斗部狭窄。
诊断性软镜镜检可观察到上尿路有无肿瘤和肿瘤形态、大小、部位,并能够直接活检。检查时,可通过窄带成像技术发现普通白光无法分辨的肿瘤病灶,降低术中漏诊率。对于低风险的上尿路尿路上皮癌如单发、表浅、<1.0 cm的肿瘤可行软镜下钬激光肿瘤融蚀术。
3.软镜钬激光内切开引流术治疗肾盂旁囊肿
(1)适应证:①有明确临床症状,对集合系统形成压迫,形成局限性肾积水;②邻近集合系统(与肾盂、漏斗部或肾盏壁邻近);③囊肿位置位于肾窦内或呈内生性生长,其他手术方式不易接近。
(2)禁忌证:为术前不能排除恶变的肾囊肿以及肾囊肿合并出血。
4.软镜在输尿管狭窄治疗中的应用
利用软镜置入导丝或者用钬激光对狭窄部位做初步切开便于插入气囊导管行气囊扩张,狭窄长度≤0.5 cm疗效更好。也有采用经皮肾通道软镜联合球囊扩张治疗复杂输尿管下段狭窄的报道。
5.软镜钬激光碎石术在特殊病例中的应用
特殊病例包括:①肾盏憩室结石、马蹄肾肾结石、异位肾合并结石、多囊肾合并结石、孤立肾较大的肾结石的治疗;②尿流改道术后输尿管结石的治疗;③小儿上尿路结石的治疗。
二、相关并发症的预防及处理
1.手术时间与并发症发生
手术操作时间长,并发症发生概率增加。有研究认为将灌注冲洗的时间控制在1 h以内可以显著降低发生严重并发症的概率。软镜碎石手术时间延长(>90 min)与结石体积(≥550 mm3)、术前未使用支架管、结石CT值≥1000 HU、术者经验的欠缺(<50例)相关。建议软镜碎石术的手术时间控制在<90 min。
2.术后感染
术后感染是软性输尿管镜最常见的并发症。预防措施如下:
(1)围术期尿路感染的治疗是预防的关键,术前抗生素的使用对降低术后尿路感染至关重要;
(2)对于结石感染合并明显梗阻的患者,可先置入输尿管支架管或者肾造瘘管引流,待感染控制后再二期手术治疗结石,术后再给予足量的敏感抗生素;
(3)术中应遵循“见脓就停”的原则,即发现脓性絮状物应立即停止手术,同时置内支架管引流;
(4)术中使用大口径软镜输送鞘,有助于降低肾盂内压力;
(5)术中灌注的原则:在维持视野清晰的前提下,尽量保持低压,低流量灌注;
(6)有些患者,即便术前尿培养无菌或术前进行预防性抗生素应用,术后仍有可能发生全身炎症反应综合征,因此术中行结石碎块细菌培养和药敏试验,对于术后选择敏感抗生素,进行有效抗感染治疗非常重要;
(7)控制手术时间,对于负荷大的大结石或鸟粪石,应采取分期手术以缩短手术时间,降低感染发生率,建议手术时间<90 min;
(8)保持术后尿路引流通畅。
3.输尿管损伤
主要为输尿管通道鞘(UAS)所致的输尿管损伤,发生率最高可达46.5%。
分为5级:黏膜出血点(0级),黏膜损伤(1级),肌层损伤但外膜尚存(2级),穿孔(3级),撕脱(4级)。其中,0级和1级为轻度损伤,超过2级为严重损伤。输尿管肌层损伤的发生率为13.3%,软镜术后输尿管狭窄的发生率仅1.4%。一旦出现输尿管损伤,术后应及时留置双J管。输尿管损伤的程度不同,双J管留置的时间不同。0级和1级的输尿管损伤,术后双J管应留置1~2周;超过2级的输尿管损伤,术后双J管应留置3~6周。
4.软镜术中出血
软性输尿管镜手术可能因各种原因损伤集合系统黏膜,导致出血。一旦出现这种情况,可退出软镜,将UAS内芯放入鞘内,观察5~10 min,让肾盂内的出血形成血凝块,压迫出血点,一旦出血停止,可继续进行手术;若视野仍不清晰,则应及时终止手术,留置双J管二期手术,避免因视野问题引起更为严重的并发症。
参考文献:中华医学会泌尿外科分会,中国泌尿系结石联盟.软性输尿管镜术中国专家共识.中华泌尿外科杂志,2016,37(8):561-565.