
膀胱肿瘤是泌尿外科最常见的肿瘤之一,其发病率在世界范围内逐年上升。膀胱癌首次诊断时大约30%为肌层浸润性膀胱癌(MIBC)。
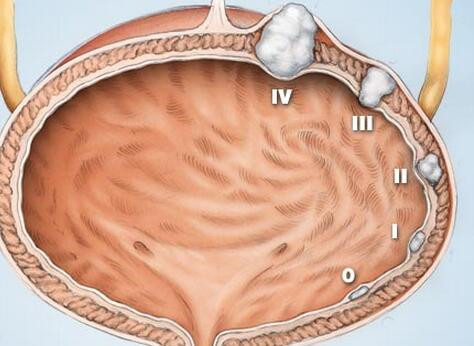
MIBC的新辅助化疗现状
目前,对于局部晚期肌层浸润和转移性的膀胱癌,NCCN指南充分肯定了新辅助化疗的作用,即对于所有身体情况允许的患者,推荐术前以铂类为主的新辅助化疗。其目的有两方面:一是控制局部病变,使肿瘤缩小、降期,改善局部治疗的疗效;二是通过消灭可能存在的术前微转移灶,有效改善长期生存。
新辅助化疗的优点包括:①可评价肿瘤对化疗的反应,对评估预后有重大意义;②可以降低肿瘤分期,缩小手术范围,从而达到保留器官的目的;③可以进行体内药物敏感试验,为后续治疗提供相关信息;④患者于术前一般状况较好,较术后能耐受更多剂量和更长疗程的化疗。
2003年,新英格兰杂志发表文章表明,对于T2-T4aN0M0期膀胱癌患者,相较于单纯行根治性膀胱切除-盆腔淋巴清扫,术前新辅助化疗能明显降低病理分期(38%患者可以通过化疗达到cT0),提高RC后5年生存率,并延长中位生存时间。Yin Ming等荟萃分析了15个术前新辅助化疗的临床试验,发现新辅助化疗可以显著改善生存预后,降低死亡风险16%。
在我国,膀胱癌新辅助化疗则起步较晚。根据中国膀胱癌联盟2018年数据统计,MIBC患者接受新辅助化疗比例不超过3%。造成这一现象的原因主要有以下几个方面:目前新辅助化疗概念模糊、会带来相关不良反应、延误手术时机,及外科医生对化疗不熟悉等。
而就目前所掌握的接受新辅助化疗患者的临床资料来看,不是所有的患者都可以耐受新辅助化疗,同时接受新辅助化疗的患者并非全部有效。临床上,化疗无效的患者不仅无治疗获益,而且要承受化疗带来的不良反应,更可能延误最佳的手术治疗时机。
此外,缺少明确的疗效预测指标,也是新辅助化疗不能够全面开展的重要原因。
MIBC的新辅助免疫治疗研究进展
与此同时,近年来肿瘤免疫治疗一直是肿瘤治疗的热点。MIBC的新辅助免疫治疗也逐渐被人们所认识。在2018年ESMO、2019年ASCO-GU及EAU等会议上,关于MIBC的新辅助免疫治疗的两项Ⅱ期临床研究(PURE-01和ABACUS)结果,令全世界泌尿肿瘤医生欢欣鼓舞。
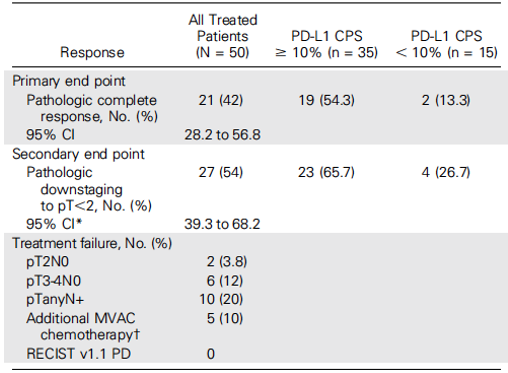
在PURE-01临床试验中,50例MIBC患者(临床分期≤T3b)每3周予200mg pembrolizumab(PD-L1抑制剂)新辅助免疫治疗,3周期后行膀胱根治性切除术。3例患者由于出现3~4级不良反应,其中1例更改为MVAC方案化疗,其余47例(94%)均完成3周期新辅助免疫治疗。术后病理结果显示,新辅助免疫治疗病理完全缓解率(pCR)可以达到42%(21/50),不差于MAVC新辅助化疗方案(38%),同时27人(54%)出现肿瘤降期。
研究还发现,54.3% PD-L1高表达患者可以到达病理完全缓解,而对应的PD-L1低表达患者比例只有13.3%。进一步分析发现,当肿瘤突变负荷(TMB)大于15 mut/Mb时,患者具有更高的病理完全缓解率。
在2019年欧洲泌尿年会上,Zaffuto Emanuele等人为验证新辅助免疫治疗的安全性,回顾性分析了802例接受膀胱根治性切除术的患者,其中61例接受过MVAC新辅助化疗,52例接受过新辅助免疫治疗,689未接受任何新辅助治疗。结果发现,虽然接受新辅助免疫治疗的患者发生发热及肠梗阻风险更高,但术前行新辅助治疗被证实是安全的,且新辅助免疫治疗较新辅助化疗在不增加手术并发症的情况下有更高的肿瘤缓解率。

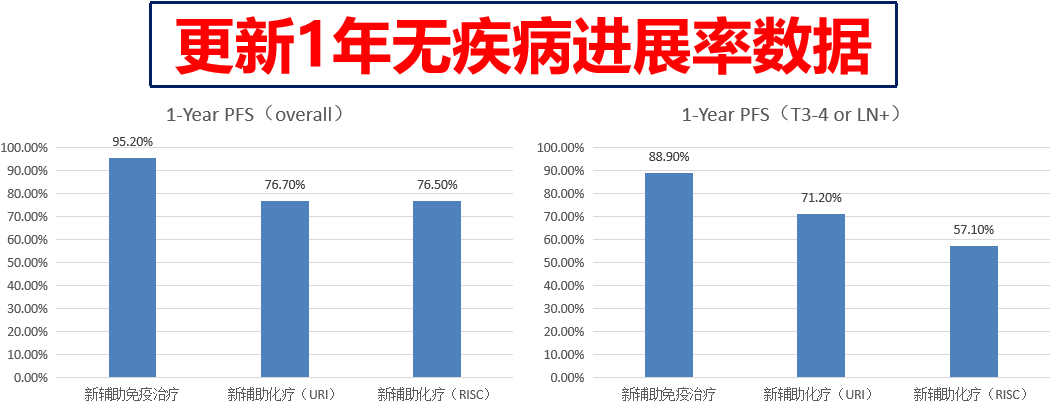
与此同时,2019年EAU更新了PURE-01临床试验术后1年无疾病进展率数据,表明接受新辅助免疫治疗的患者较新辅助化疗患者具有更高的1年无疾病进展率(95.2% vs 76.7%)。
与PURE-01相类似,ABACUS是一项研究PD-L1抑制剂Atezolizumab作为膀胱癌新辅助免疫治疗药物有效性及安全性的二期临床实验。共纳入74例T2-4N0M0期MIBC患者,在手术前予2周期Atezolizumab新辅助免疫治疗(1200 mg Q3),结果20%的患者只进行了1周期治疗(15例)。在最终取得病理标本的68例患者中(67例行膀胱切除术,1例术前肿瘤进展),pCR率为20/68(29%),39%的患者肿瘤降期为NMIBC。进一步分析纳入患者PD-L1表达水平,发现PD-L1高表达组中40%患者可以达到pCR,而对应的PD-L1低表达组这一比例只有16%。表明Atezolizumab在膀胱癌新辅助免疫治疗中可以发挥重要作用。

新辅助免疫治疗疗效的预测指标
随着新辅助免疫治疗临床试验的开展,如何在治疗前预测疗效,寻找疗效预测标志物也逐渐被人们所重视。在PURE-01试验中,当患者肿瘤突变负荷大于15 mut/Mb,则具有跟高的病理完全缓解率,且TMB与DDR突变显著相关。
2018年Journal of Clinical Oncology上发表的一篇文章,回顾分析了60例接受nivolumab或atezolizumab治疗的晚期膀胱癌患者,分析其DDR突变及有害DDR突变对客观缓解率(ORR)、PFS及OS的影响。结果发现,内脏转移和DDR突变是ORR、PFS及OS的独立预后因素,DDR突变的患者可以获得更好的PFS和OS,预示DDR突变对预测免疫治疗疗效有重大关联。
总之,对于MIBC,新辅助化疗+根治性膀胱全切术目前仍然是一线治疗方案。新辅助免疫治疗虽然取得了令人鼓舞的II期临床试验结果,但仍需进一步深入研究及数据支持其疗效。未来肌层浸润膀胱癌新辅助免疫治疗+化疗的临床试验结果同样令人期待。
参考文献
[1] Grossman HB, Natale RB, Tangen CM, et al. Neoadjuvant chemotherapy plus cystectomy compared with cystectomy alone for locally advanced bladder cancer [J]. The New England journal of medicine, 2003, 349(9):859-866.
[2]Necchi A, Anichini A, Raggi D, et al. Pembrolizumab as Neoadjuvant Therapy Before Radical Cystectomy in Patients With Muscle-Invasive Urothelial Bladder Carcinoma (PURE-01): An Open-Label, Single-Arm, Phase II Study [J]. Journal of clinical oncology : official journal of the American Society of Clinical Oncology, 2018:Jco1801148.
[3]Teo MY, Seier K, Ostrovnaya I, et al. Alterations in DNA Damage Response and Repair Genes as Potential Marker of Clinical Benefit From PD-1/PD-L1 Blockade in Advanced Urothelial Cancers [J]. Journal of clinical oncology : official journal of the American Society of Clinical Oncology, 2018, 36(17):1685-1694.